Les différents implants, le plus souvent dans le domaine de la chirurgie osseuse, subissent l’adhésion de bactéries ou champignons, d’où biofilm, d’où infections potentielles. “Il suffit” de traiter au laser ces surfaces, pour les rendre naturellement antibiotiques …
Des chercheurs du RMIT en Australie ont développé une approche sans médicament pour tuer les bactéries et les champignons susceptibles d’infecter les surfaces des implants médicaux. Ces agents pathogènes peuvent provoquer des infections graves et difficiles à traiter autour des implants médicaux, nécessitant parfois le retrait de l’implant.
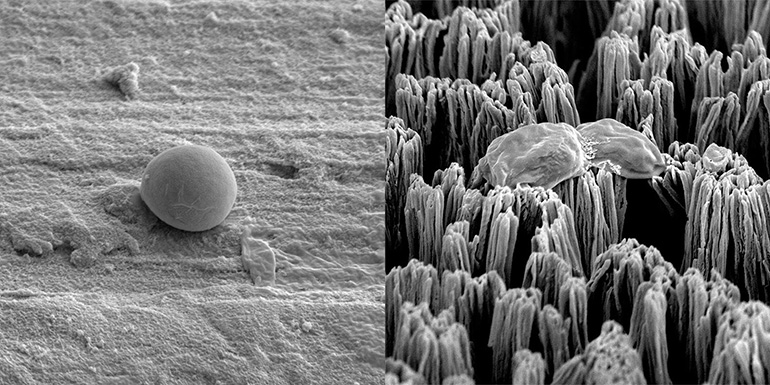
En outre, de nombreux microbes sont de plus en plus résistants aux antibiotiques courants, ce qui souligne la nécessité d’approches sans médicaments. Cette nouvelle technique s’inspire des nanopiliers présents sur les ailes des libellules, qui peuvent embrocher les cellules microbiennes et les tuer. Les chercheurs ont utilisé une technique de gravure au plasma relativement simple pour créer de tels nanopiliers sur des surfaces en titane et ont testé leur capacité à tuer les cellules Candida multirésistantes , un pathogène fongique à l’origine de nombreuses infections liées aux dispositifs médicaux.
Les implants médicaux peuvent remédier à de nombreuses situations cliniques malheureuses, mais ils peuvent également abriter des microbes qui peuvent coloniser les surfaces du dispositif après implantation. Cela conduit généralement à une vilaine infection, qui est souvent compliquée par la formation d’un biofilm, et peut nécessiter le retrait éventuel de l’implant. La résistance aux médicaments antimicrobiens est une autre complication, et cela a inspiré ces chercheurs à créer une modification de surface sans médicament qui peut tuer les microbes sans discernement.
Ils ont utilisé une technique de gravure au plasma pour créer de minuscules piliers sur du titane, utilisé dans de nombreux implants médicaux. Les minuscules pointes ont approximativement la hauteur d’une cellule bactérienne et, lorsqu’une cellule se dépose à la surface, les pointes peuvent entraîner des perforations dans la cellule pouvant entraîner sa mort. Dans les études menées jusqu’à présent, les chercheurs ont montré que si la cellule ne meurt pas complètement, elle périra quand même un peu plus tard en raison des dommages qu’elle a subis.
“Le fait que les cellules soient mortes après un premier contact avec la surface – certaines par rupture et d’autres par mort cellulaire programmée peu de temps après – suggère que la résistance à ces surfaces ne se développera pas”, a déclaré Elena Ivanova, chercheuse impliquée dans l’étude. « Il s’agit d’une découverte importante qui suggère également que la manière dont nous mesurons l’efficacité des surfaces antimicrobiennes pourrait devoir être repensée. Cette dernière étude suggère qu’il n’est peut-être pas entièrement nécessaire que toutes les surfaces éliminent tous les agents pathogènes immédiatement après contact si nous pouvons montrer que les surfaces provoquent la mort cellulaire programmée dans les cellules survivantes, ce qui signifie qu’elles meurent malgré tout.
