Quand on dit eau, on pense H20, molécule simple, universelle, pleine de malice et de capacités. Mais pour en expliquer certaines propriétés, il faut creuser plus loin...

L’eau est omniprésente dans l’organisme, sous forme circulante (sang, lymphe, liquide céphalo-rachidien), sous forme extracellulaire (c’est l’eau du conjonctif), et sous forme intracellulaire, où les molécules sont comprimées et forment un réseau dont on est loin de connaître tous les secrets…
La répartition électronique dans une molécule d’eau fait qu’elle présente une symétrie bilatérale : deux atomes d’hydrogènes (ou protons) situés d’un même coté par rapport à l’oxygène, ce qui donne à la molécule une fonction de dipole.
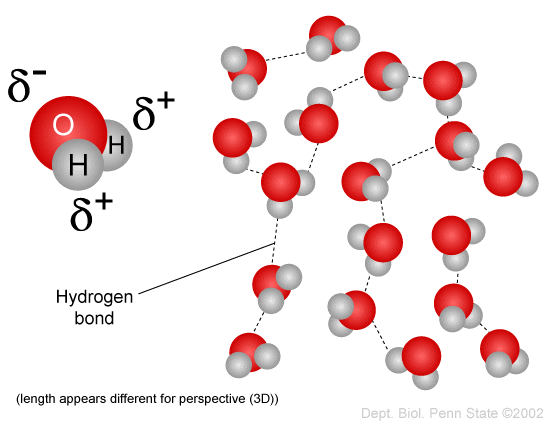
Ce dipole est très stable, ce qui suffit par lui-même à expliquer bien des caractéristiques si particulières de l’eau.
En phase liquide, l’eau voit ses molécules animées de mouvements impulsés par les liaisons hydrogène O<>H qui se font et se défont au rythme de 500 milliards de fois par seconde, ce qui entraîne une fluidité très spécifique (et unique !) et la possibilité de créer des groupements plus organisés (domaines de cohérence), en particulier lorsque l’eau se trouve au contact d’autres molécules.
Les molécules d’eau s’organisent autour des solutés (cristaux solubles) pour former une couche dite de salvation, qui va accompagner l’ion du soluté (chlorure, magnésium, etc..) dans ses parcours.
Dans le cas des substances solubles polaires (sucres), une même couche de salvation s’organise, dont l’épaisseur dépend à la fois de la charge de l’ion et de sa taille.
Ceci est très important en biologie : l’introduction d’ions dans une solution colloïdale, où de grosses molécules sont solubilisées dans l’eau, entraine la captation progressive des molécules d’eau au détriment des macromolécules, et la floculation de ces dernières. C’est le phénomène de salting-out, bien connu par exemple en œnologie (technique du collage), mais aussi redoutable en médecine (empoisonnements ophidiens, chocs anaphylactiques).
Des macromolécules bien hydratées
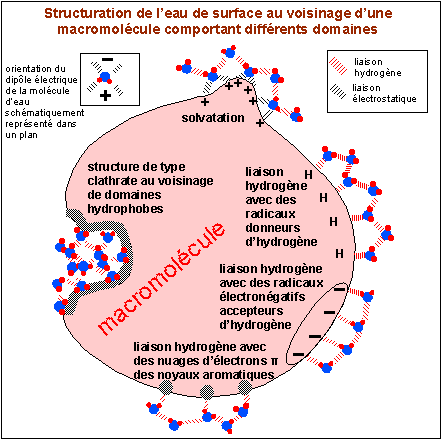
Les macromolécules solides, comme les protéines, présentent sur leur surface de nombreux sites hydrophiles qui peuvent capter des molécules d’eau, soit selon les forces électrostatiques, soit selon des liaisons hydrogène.
Il existe donc une première couche, au contact immédiat, puis une seconde couche, puis encore une troisième, de molécules d’eau, selon des lignes de force axées sur ces sites hydrophiles.
Cette eau est sous influence de la macromolécule, et en même temps, elle agit sur elle : c’est l’eau structurée.
Les macromolécules (lipides membranaires, acides nucléiques) présentent également sur leur surface des zone non polaires qui n’attirent pas l’eau : il peut alors s’y glisser des groupements d’eau en clathrates, véritables cages très solides, quasi cristallines, qui repoussent les sites hydrophobes vers l’intérieur de la molécule.
La complexité occulte de l’eau
Jean-Marie Pierre Le Chapellier nous a instruit pendant des années lors des Journées de l’Eau toulousaines, nous lui empruntons ici son très rare savoir.
Dans l’eau, même dans une eau très pure, il n’y a pas que de l’eau. Il y a des molécules H2O, bien sûr, mais également du vide, le vide physique aqueux, et puis il y a forcément un reliquat de gaz dissous, toutes petites molécules apolaires qui passent inaperçues jusqu’au moment où …( Thèse de Philippe Vallée)
Le vide physique : les liaisons H devraient précipiter entre elles les molécules d’eau, et ce n’est pas le cas : c’est donc qu’il existe une énergie de répulsion pour équilibrer cette liaison. Cette énergie est prélevée du vide qui possède des propriétés structurelles et énergétiques. D’où une équation nouvelle (et peu admise par la physique classique) :
Eau = n(H2O) + (vide physique aqueux).
Ce vide physique aqueux n’a rien à voir avec un espace vide et plat de la physique. Il est plus proche du concept topologique impliquant courbure, connexions et torsion. Il peut être défini comme champ fondamental qui permet l’existence de l’eau avec sa structure et ses propriétés sous deux formes :
- les clusters (ou petits groupements) au voisinage d’une molécule ou d’une paroi (eau d’hydratation). Dans ce cas, l’environnement topologique est lié à l’environnement même de la paroi.
- Dans un volume d’eau « libre », les environnements individuels des molécules sont fondus dans un même vide quantique aqueux dont la nature est thermodynamique et topologique.
La structure du vide physique aqueux évolue avec l’âge (déshydratation progressive de la substance fondamentale), mais se trouve également modifiée par l’intervention d’énergies et des effets de champs électromagnétiques, de même qu’un éclair dans le ciel peut venir à briser l’organisation des nuages et à les transformer en pluie…
Inversement, on peut envisager d’agir contre le vieillissement par l’action judicieuse de champs magnétiques. C’est un des thèmes de recherches de JM Le Chapellier.
En effet, un champ magnétique de faible intensité peut affecter la densité ionique autour des colloïdes, provoquant ainsi un redéploiement des macromolécules concernées.
Les gaz de l’eau : le long des surfaces hydrophobes s’accumulent des bulles de gaz avec leur double couche hydratée, qui se libèrent sous l’action d’un champ magnétique. Une application immédiate est le détartrage magnétique des tuyauteries (à grande échelle), mais le même phénomène se produit au sein même du conjonctif, avec des conséquences évidentes sur le pH de la substance fondamentale, puisque le gaz en question est majoritairement du gaz carbonique, accompagné d’oxyde nitrique.
Angelina Viva
